Table of Contents
في أعماق أجهزتنا الهضمية، يعيش مجتمع صاخب من تريليونات البكتيريا التي نعتبرها عادةً حلفاءنا الأوفياء في هضم الطعام وتعزيز المناعة. ولكن، كما هو الحال في أي قصة معقدة، يوجد خونة بين الصفوف. بعض سلالات بكتيريا الإشريكية القولونية (E. coli) لا تكتفي بالتعايش السلمي، بل تنتج سماً دقيقاً وفتاكاً يُعرف بـ “كوليباكتين” (Colibactin). لطالما حير هذا السم العلماء بقدرته الغريبة على إتلاف الحمض النووي البشري، ولكن الآلية الدقيقة ظلت لغزاً غامضاً لسنوات. اليوم، وبفضل كيمياء مبتكرة، كشف العلماء أخيراً كيف يوجه هذا السم “رؤوساً حربية” كيميائية لتمزيق شفرتنا الوراثية، مسبباً طفرات ترتبط ارتباطاً وثيقاً بسرطان القولون.
عناق قاتل للحمض النووي
قصة الكوليباكتين ليست جديدة تماماً، فمنذ اكتشافه عام 2006، تراكمت الأدلة التي تشير إلى دوره في تطور سرطان القولون، وهو مرض يصيب شخصاً من كل 25 شخصاً في الولايات المتحدة خلال حياتهم. لكن الجديد والمثير هو ما كشفته دراسة نشرت في دورية Science، حيث تمكنت الكيميائية إميلي بالسكوس (Emily Balskus) وفريقها من جامعة هارفارد من فك شفرة الهيكل الكيميائي لهذا السم وكيفية عمله.

أظهرت الدراسة أن الكوليباكتين يمتلك هيكلاً مصمماً ببراعة خبيثة ليعانق الحمض النووي (DNA). إنه لا يهاجم بشكل عشوائي، بل يمتلك “مجموعات كيميائية” (Warheads) شديدة الفعالية لدرجة أن العلماء وصفوها بالرؤوس الحربية. هذه الرؤوس تسمح للسم بالارتباط بتسلسلات محددة جداً من الحمض النووي، مما يؤدي إلى إحداث ضرر دقيق ومستهدف.
كيف تعمل “الرؤوس الحربية” البكتيرية؟
يكمن خطر الكوليباكتين في قدرته على التسلل. يمتلك هذا الجزيء قلباً غير مستقر يحتوي على مجموعة نيتروجينية مشحونة بالبروتونات الموجبة، مما يساعده على التعرف على تسلسلات معينة من الحمض النووي والالتصاق بها. وبمجرد أن يستقر في مكانه، يمد ذراعيه الطويلتين المزودتين بتلك “الرؤوس الحربية” — وهي عبارة عن مثلثات كيميائية مكونة من ثلاث ذرات كربون.
هذا التصميم الهيكلي هو وصفة للكارثة؛ فهو يسمح للكوليباكتين بالإمساك بكلا شريطي الحلزون المزدوج للحمض النووي وربطهما معاً بقوة. هذا ما يسميه العلماء “الربط المتصالب بين الشرائط” (Interstrand cross-link). تخيل أنك وضعت مفك براغي معدني بين تروس آلة تدور؛ هذا بالضبط ما يفعله السم. إنه يمنع الحمض النووي من الانفكاك لغرض النسخ أو القراءة بواسطة آلات صنع البروتين في الخلية.
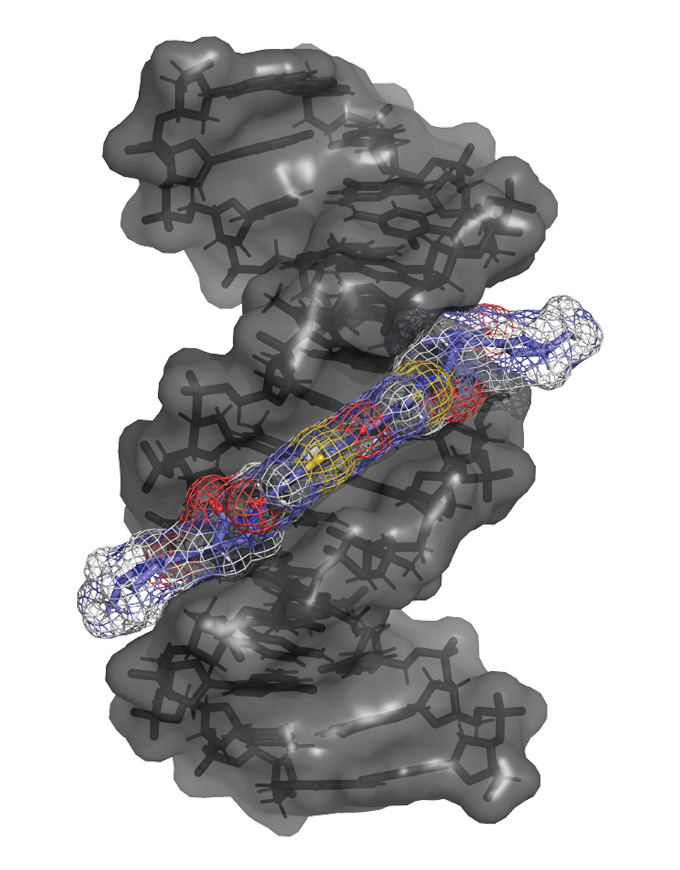
تحاول الخلية البشرية جاهدة إصلاح هذا الضرر، لكن عملية الإصلاح غالباً ما تكون فوضوية وغير دقيقة، مما يترك وراءه ندوباً دائمة في الشفرة الوراثية: طفرات محددة تظهر في “بصمة” جينية توجد في 5 إلى 20 بالمائة من حالات سرطان القولون.
مصيدة ذكية لجزيء مراوغ
لماذا استغرق الأمر نحو 20 عاماً لكشف هذا الهيكل؟ يجيب أورلاندو شارير (Orlando Schärer)، الكيميائي وعالم الأحياء بجامعة بيتسبرغ، بأن السبب يكمن في عدم استقرار الجزيء. يقول شارير: «لأنه غير مستقر، لم يتمكن أحد من عزله فعلياً». الكوليباكتين الحر يتحلل بسرعة كبيرة في المختبر، مما جعل دراسته بالطرق التقليدية شبه مستحيلة.
لكن فريق إميلي بالسكوس تحايل على هذه المشكلة بطريقة غير تقليدية. بدلاً من محاولة تنقية الجزيء في أنبوب اختبار، استخدموا البكتيريا الحية نفسها كمصنع كيميائي. لقد حددوا تسلسلات الحمض النووي المفضلة للكوليباكتين واستخدموها كـ “طُعم”. عندما التقط السم الطعم وارتبط به، قام الباحثون بتثبيت المركب وتحليل هيكله باستخدام تقنيات متطورة مثل قياس الطيف الكتلي والرنين المغناطيسي النووي. تصف بالسكوس هذه اللحظة قائلة: «هذا هو أقرب ما وصلنا إليه لحل لغز هيكل الكوليباكتين، وهي رحلة استغرقت المجال العلمي قرابة 20 عاماً».
من المختبر إلى العيادة: الأمل في الكشف المبكر
إن فهم الآلية الدقيقة لعمل الكوليباكتين ليس مجرد إنجاز أكاديمي؛ بل هو خطوة حيوية نحو تطبيقات طبية منقذة للحياة. إن الربط القوي بين هذا السم و”البصمات الطفرية” المحددة في سرطان القولون يعني أن العلماء قد يتمكنون قريباً من تطوير اختبارات للكشف عن التعرض للكوليباكتين قبل وقت طويل من ظهور السرطان.
هذه الاكتشافات قد تسلح الأطباء بأدوات أفضل لتقييم مخاطر الإصابة بالسرطان لدى المرضى، مما يفتح الباب أمام استراتيجيات وقائية تستهدف هذه البكتيريا “الخائنة” في أمعائنا قبل أن تشن هجومها المدمر.
